
西安交通大学郭晓宇、苏彦文、马瑞等学者在国际权威期刊 Chemical Engineering Journal 发表的研究 “Dual-functional 3D-printed polyetheretherketone scaffolds with immunomodulatory nano-calcium silicate/interleukin-4 coating synergistically enhance osteogenesis through macrophage M2 polarization and NF-κB pathway suppression”,提出了一种将免疫调控与成骨诱导协同整合于PEEK支架的创新策略。
聚醚醚酮(PEEK)凭借其与人体骨骼相近的力学特性和良好的影像学兼容性,在骨科植入物领域占据重要地位。然而,其生物惰性导致的骨整合能力不足,始终是制约其更广泛应用的关键瓶颈。如何在保留PEEK固有优势的同时,赋予其引导组织再生的能力,成为该领域的研究热点。
01
结构先行:
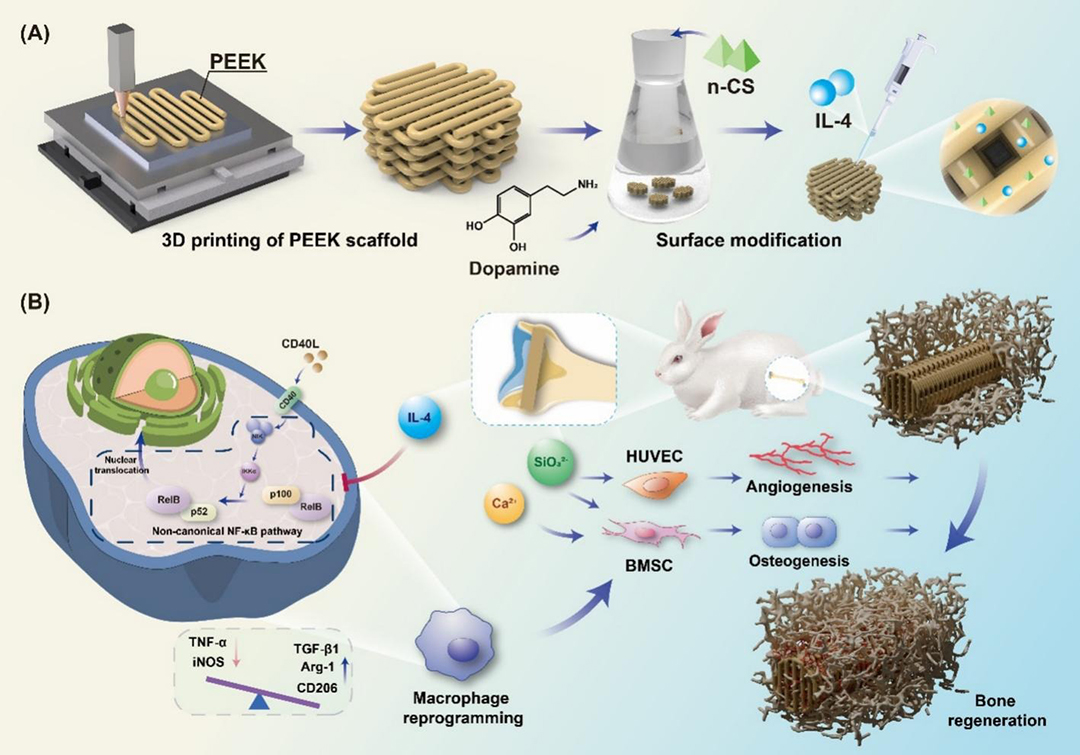
3D打印构建“骨仿生”微环境
02
表面赋能:
PDA介导的“三步嫁接”技术
03
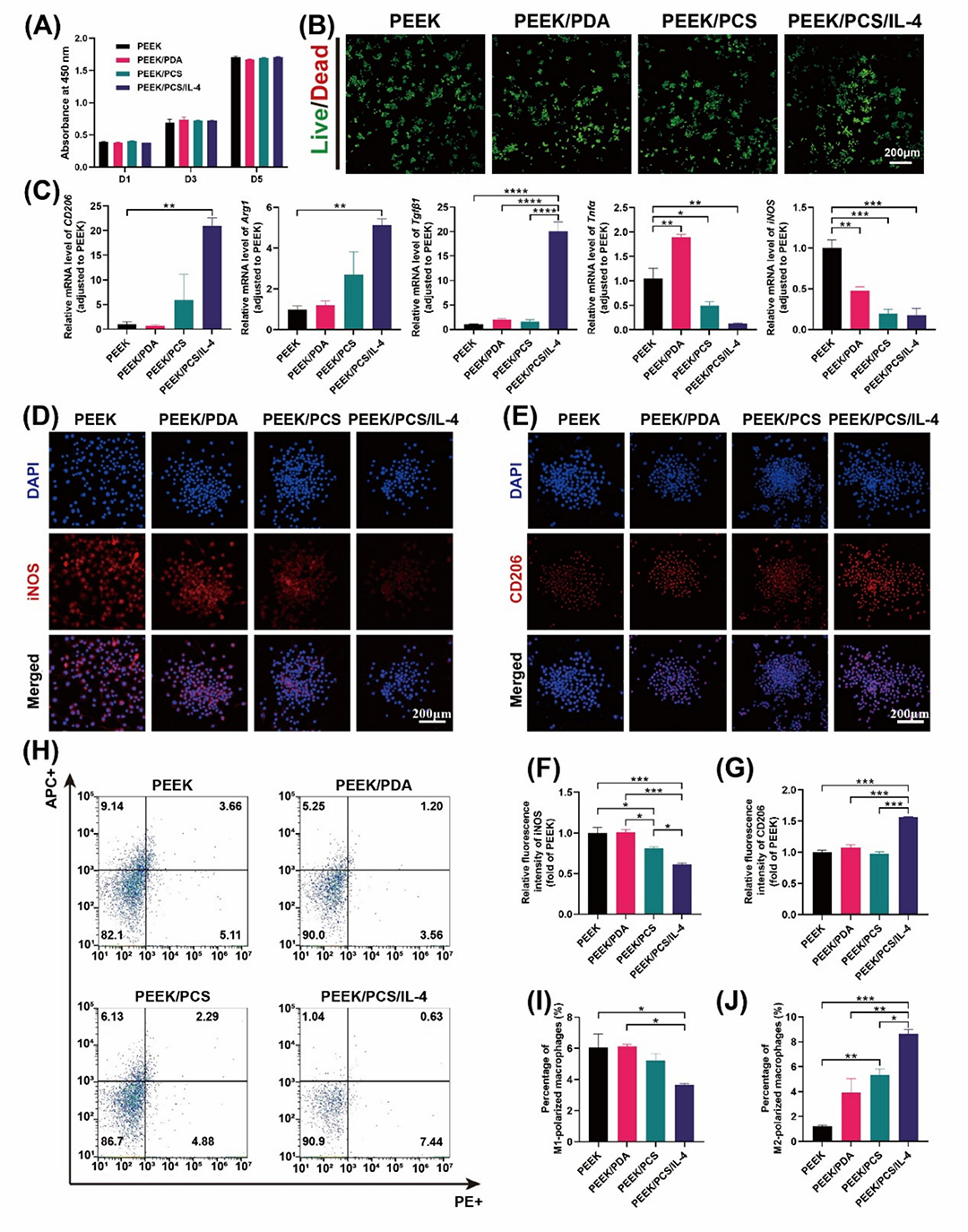
机制解析:
巨噬细胞极化的分子通路
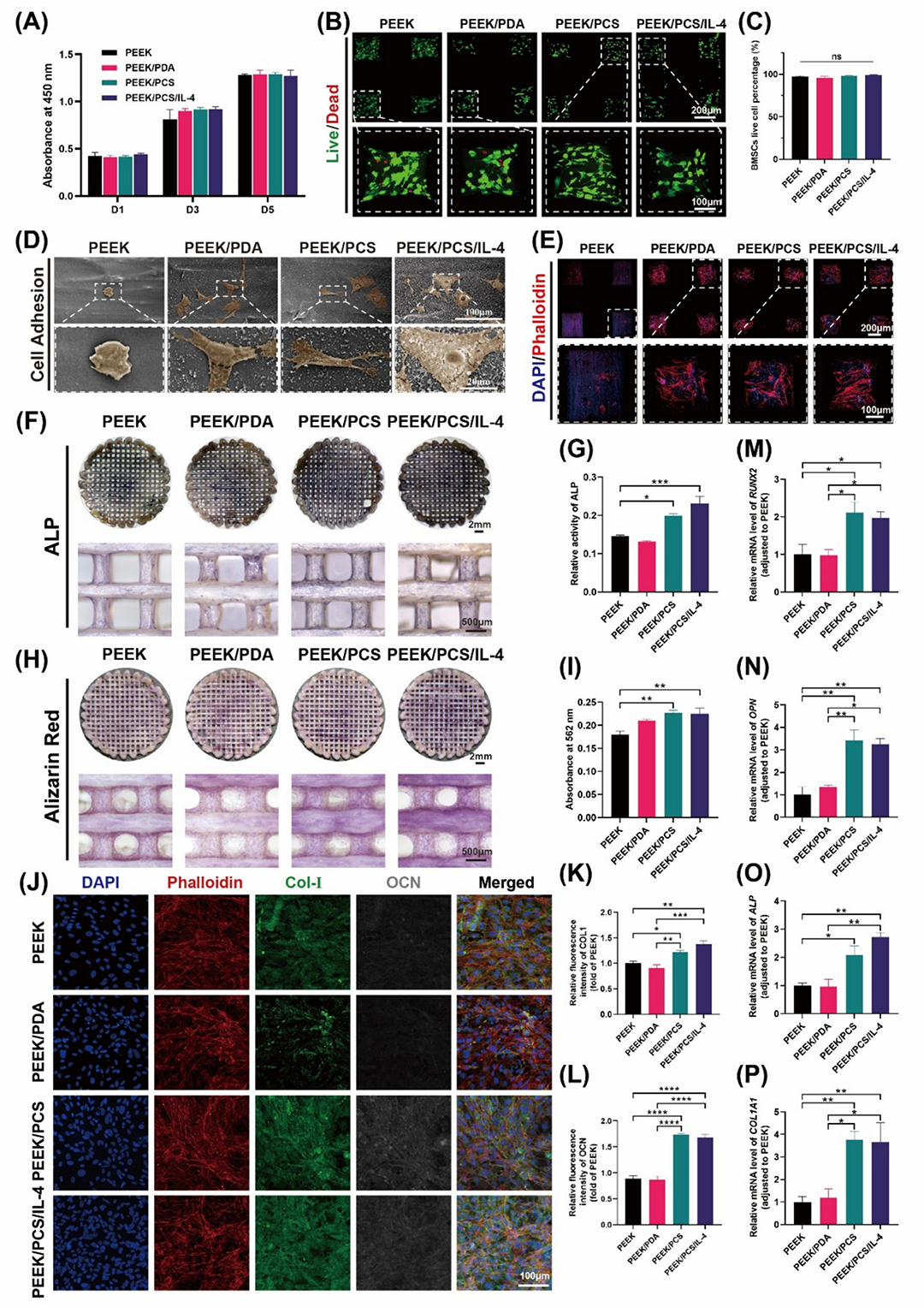
04
功能验证:
多维度评估修复效能
05
结语:
免疫-成骨新范式



























 首页
首页 电话咨询
电话咨询 留言
留言







